국내최초통합줄기세포은행
Bio Insurance
국내최초통합줄기세포은행
Bio Insurance
국내최초통합줄기세포은행
Bio Insurance
국내최초통합줄기세포은행
Bio Insurance
국내최초통합줄기세포은행
Bio Insurance
Global CHA Network
| 구분 | 망막 색소상피세포(MA09-hRPE) | ||
| 적용질환 | 스타가르트병(SMD) | 진행된위축성이관련황반변성증(AMD) | 근시성황반변성증(MMD) |
| 개발의의 | - 세계 최초 배아줄기세포 유래 세포치료제 상용화 - 황반변성 질환에 대한 근본적인 치료 가능 |
||
| 질환특성 | - 유전자 돌연변이로 인해 실명 유발 | - 고령자에게서 망막 퇴화로 시력 소실과 실명 유발 - 노인인구 증가와 함께 비례하여 증가 추세 |
- 근시가 심한 사람들에게서 나타나는 비정상적인 망막 변화 |
| 진행경과 | - 2009년 미국 ACT사와 기술제휴를 통해 파이프라인도입 - 2010년 희귀약품지정 (미국FDA)으로 다양한 혜택 보장 (최대 7년 동안 마케팅 독점 승인,세금공제,임상시험 자금지원,FDA승인 가속화, 약품승인) |
||
| - 미국 FDA 임상 승인(2010.11) - 한국 MFDS 임상 승인(2011.05) |
- 미국 FDA 임상 승인(2011.01) - 한국 MFDS 임상 승인(2012.05) |
- 미국 FDA 임상 승인(2013.02) - 한국 MFDS 임상 승인(2013.10) |
|
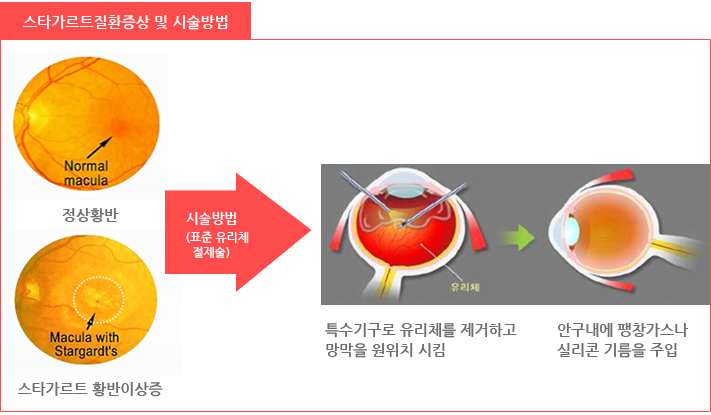
| 시술방법 | - 1단계 : 표준 유리체 절제술 시행 - 2단계 : 망막 하 배아줄기세포 유래 망막상피세포 이식 |
||
| 임상결과 | - 국내 임상참가자의 시각 또는 시기능 호전 - 미국/유럽 임상참가자 시력 회복(일반 시력표 기준 0.05에서 0.5로 회복) |
- 임상진행중 | |